Cục Quản lý Dược căn cứ vào các quy chế dược hiện hành của Việt Nam và công văn số 523/VKNT-KHTH đề ngày 14/10/2019 của Viện kiểm nghiệm thuốc Thành phố Hồ Chí Minh gửi kèm phiếu kiểm nghiệm số 1629/VKNYC2019 và Phiếu kiểm nghiệm số 1630/VKN-YC2019 ngày 14/10/2019 báo cáo kết quả lấy mẫu bổ sung đối với lô thuốc Viên nén LIV-Z Tablets, số lô: MYTHB1801, NSX: 06/03/2018, HD: 05/03/2020 nêu trên.
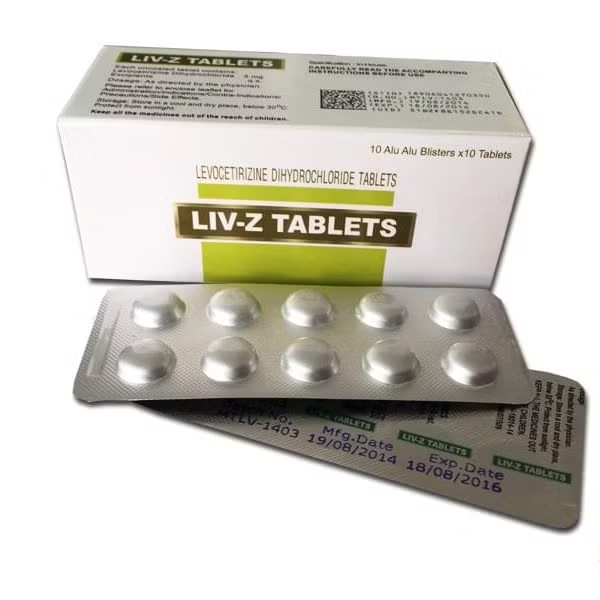 |
| Cục Quản lý Dược yêu cầu tạm dừng nhập khẩu, phân phối, sử dụng mặt hàng thuốc Viên nén LIV-Z Tablets. Ảnh minh họa |
Theo đó, khi tiến hành phân tích bổ sung bằng phương pháp HPLC sử dụng cột tách đồng phân, thì kết quả sắc ký đồ của mẫu thuốc xuất hiện 2 pic: R-Cetirizin và Levocetirizin tương tự sắc ký đồ của Cetirizin.
Sau khi xem xét hồ sơ kiểm nghiệm và các tài liệu liên quan, nhận thấy, Levocetirizin là một trong 2 thành phần quang học của Cetirizin, mẫu thuốc chứa Cetirizin.
Vì vậy, để đảm bảo chất lượng, an toàn và hiệu quả điều trị của thuốc và có đầy đủ căn cứ xử lý tiếp theo, Cục Quản lý Dược thông báo tạm dừng nhập khẩu, phân phối, sử dụng mặt hàng thuốc Viên nén LIV-Z Tablets (Levocetirizine dihydrochloride 5mg) do Công ty Maxtar Bio-Genics - India sản xuất.
Yêu cầu Công ty cổ phần dược liệu Trung ương 2 phối hợp với Công ty Maxtar Bio-Genics - India (India), các công ty của Việt Nam nhập khẩu và phân phối thuốc LIV-Z tablets: Tạm dừng nhập khẩu, phân phối các lô thuốc Viên nén LIV-Z Tablets (Levocetirizine dihydrochloride 5mg) Công ty MaxtarBio-Genics -India sản xuất.
Trong thời hạn 48h kể từ ngày ký Công văn này, gửi thông báo tạm dừng phân phối, sử dụng tới các cơ sở bán buôn, bán lẻ, sử dụng đã được cung ứng thuốc Viên nén LIV-Z Tablets do Công ty Maxtar Bio-Genics - India (India) sản xuất nêu trên.
Báo cáo về Cục Quản lý Dược trước 12h ngày 22/10/2019 về việc cung ứng, nhập khẩu vào Việt Nam thuốc Viên nén LIV-Z Tablets (Levocetirizine dihydrochloride 5mg) trong thời gian từ 01/6/2017 đến nay (số lô, ngày sản xuất, ngày hết hạn, ngày nhập, số lượng nhập khẩu và tình hình phân phối thuốc).
Bên cạnh đó, phối hợp với các cơ quan kiểm tra chất lượng, cơ quan kiểm nghiệm thuốc nhà nước tiến hành lấy mẫu thuốc của tất cả các lô thuốc LIV-Z Tablets (Levocetirỉzine dihydrochloride 5mg);
Gửi mẫu tới Viện Kiểm nghiệm thuốc Trung ương hoặc Viện Kiểm nghiệm thuốc Thành phố Hồ Chí Minh để tiến hành phân tích định tính và định lượng thành phần hoạt chất của thuốc.
Đồng thời, đề nghị Viện Kiểm nghiệm thuốc Trung ương, Viện Kiểm nghiệm thuốc Thành phố Hồ Chí Minh, ưu tiên tiến hành lấy mẫu để kiểm tra chất lượng đối với ít nhất 02 lô thuốc Viên nén LIV-Z Tablets (Levocetirizine dihydrochloride 5mg) do Công ty Maxtar Bio-Genics - India (India) sản xuất và tiến hành phân tích định tính, định lượng thành phần hoạt chất của thuốc (phân biệt Levocetirizin và Cetirizin).
Báo cáo kết quả về Cục Quản lý Dược để có căn cứ xử lý tiếp theo.
Ngoài ra, Sở Y tế các tỉnh thành phố trực thuộc Trung ương, Y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc tạm dùng phân phối, sử dụng thuốc Viên nén LIV-Z Tablets (Levocetirizine dihydrochloride 5mg) nêu trên, kiểm tra và giám sát các đơn vị thực hiện thông báo này; xử lý những đơn vị vi phạm theo quy định hiện hành; báo cáo về Cục Quản lý Dược và các cơ quan chức năng có liên quan.